
(来源:小张聊科研)赣州达慧
传统的代谢研究聚焦于能量与物质合成,而最新的前沿研究将代谢物和代谢酶推向了信号传导与精准调控的核心地位,下面我们就来总结一下这四种模式,并介绍一些有意思的代谢物。
模式一:代谢物介导的蛋白翻译后修饰
核心思想:代谢物作为“分子标签”,直接共价修饰蛋白质,快速改变其功能。
代谢物不再仅仅是代谢通路的中间体,它可以直接作为修饰基团的供体,在酶的催化下共价连接到靶蛋白的特定氨基酸上,从而精确、快速地调控该蛋白的活性、稳定性、亚细胞定位及与其他分子的相互作用。这种机制将细胞内瞬时的代谢状态变化,直接转化为特定的蛋白质功能指令。
经典案例:乳酸化修饰乳酸曾长期被视为糖酵解的终产物,在M1型巨噬细胞中,高水平的乳酸可作为前体,诱导组蛋白H3第18位赖氨酸发生乳酸化修饰,这种乳酸化修饰能直接激活与伤口修复相关的基因表达,驱动巨噬细胞从促炎状态向修复状态转变。这表明乳酸通过蛋白质乳酸化修饰,成为了连接细胞代谢与免疫表观遗传调控的关键信号分子。
当然,这两年蛋白乳酸化修饰的研究已经从组蛋白变为非组蛋白的修饰,如转录因子、RNA结合蛋白等。
模式二:代谢物影响蛋白-蛋白互作赣州达慧
核心思想:代谢物作为“别构开关”,非共价地调控蛋白质复合物的组装与解离。
代谢物通过非共价方式(别构效应)结合某个蛋白质上,诱导其构象发生变化。这种变化犹如一个分子开关,增强或抑制该蛋白与其他伙伴(如另一个蛋白或RNA)的结合能力,从而精密地开启或中断下游信号通路。这种模式允许细胞根据代谢物浓度对信号流进行微调。
经典案例:琥珀酸调控HIF-1α稳定性在缺氧的巨噬细胞中,累积的琥珀酸可抑制脯氨酰羟化酶(PHDs)的活性。PHDs在常氧下会羟基化转录因子HIF-1α,致其被降解。琥珀酸的抑制破坏了PHDs与HIF-1α之间的正常“识别-降解”互作,导致HIF-1α稳定存在并入核,与HIF-1β结合形成活性转录复合物,启动IL-1β等炎症因子基因的强烈表达。琥珀酸在此扮演了“炎症信号放大器”的角色。
模式三:代谢物的表观遗传调控(非PTM方式)
核心思想:代谢物作为表观遗传修饰酶的“燃料”或“刹车”,全局性调控基因表达程序。
此模式聚焦于代谢物作为必需辅因子或竞争性抑制剂,通过非共价结合来动态调节表观遗传修饰酶(如甲基转移酶、去甲基化酶、乙酰化酶等)的活性。代谢物浓度的波动直接决定了全基因组范围内表观遗传标记(如DNA甲基化、组蛋白甲基化)的书写与擦除效率,使基因表达能够对细胞内外代谢环境做出灵敏而全局性的响应。
经典案例:α-KG/TET与肿瘤发生α-酮戊二酸(α-KG)是三羧酸循环中间体,也是TET家族DNA去甲基化酶的必需辅因子,其浓度直接促进DNA去甲基化。而在某些肿瘤中,突变的异柠檬酸脱氢酶(IDH)会产生“癌代谢物”2-羟基戊二酸(2-HG),其结构与α-KG相似,能竞争性抑制TET酶活性,导致DNA出现全局性超甲基化表型,进而驱动细胞癌变。在此,代谢物通过充当“辅因子”与“抑制剂”,直接塑造了疾病的表观遗传图谱。
模式四:代谢酶的“兼职”功能
核心思想:代谢酶在特定条件下“不务正业”,发挥与其经典催化功能无关的调控作用。
机制详解:许多代谢酶具备“兼职”功能。它们可以通过亚细胞移位、与其他蛋白相互作用或发生特定的翻译后修饰等方式,在非代谢场景下(如细胞核、细胞骨架)扮演转录共调节因子、蛋白激酶、RNA结合蛋白等新角色,使代谢酶成为整合代谢与细胞命运决策的枢纽。
经典案例:PKM2的核功能糖酵解关键酶丙酮酸激酶M2(PKM2)在肿瘤细胞中可进入细胞核。在核内,它暂时“搁置”其催化糖酵解的功能,转而作为一种蛋白激酶,直接磷酸化组蛋白H3,进而激活包括细胞周期蛋白在内的多个增殖相关基因的转录。这种“催化活性”与“调控功能”的分离,使PKM2成为连接 Warburg 效应与肿瘤细胞无限增殖的关键节点。
一些有研究空间的代谢物
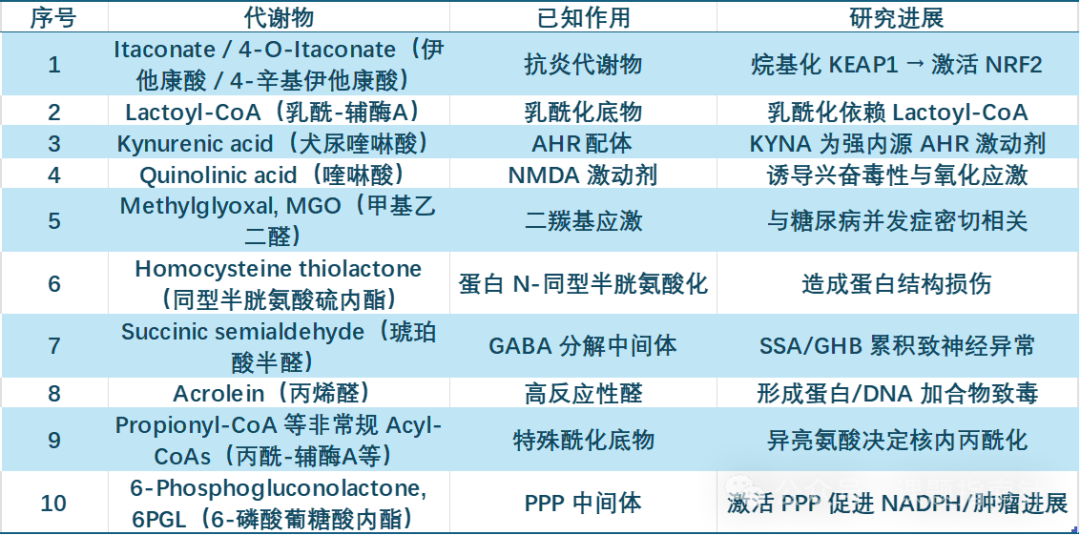
基金申请联系Bruin@解颐生物赣州达慧
 ]article_adlist-->
]article_adlist-->
 海量资讯、精准解读,尽在新浪财经APP
海量资讯、精准解读,尽在新浪财经APP
尚红网提示:文章来自网络,不代表本站观点。



